Fotosymbioza u słodkowodnych orzęsków
 Symbiozę możemy zdefiniować jako długotrwałą relację dwóch lub więcej organizmów. Jedną z najlepiej zbadanych symbioz jest ta między koralowcami i jednokomórkowymi glonami. W tym układzie, fotosyntetyzujący symbiont wytwarza cukry, z których korzysta gospodarz, w zamian zapewniając symbiontowi schronienie. Taki rodzaj symbiozy między cudzożywnym gospodarzem i glonem nazywany jest fotosymbiozą. Jest ona powszechna w środowiskach morskich, gdzie symbiotyczne glony mają znaczny wkład w produkcję pierwotną i stanowią istotną część biomasy ekosystemów. Fotosymbiozy umożliwiają wzrost gospodarza w niekorzystnych warunkach umożliwiając mu pozyskiwanie deficytowych składników od partnera. W roli gospodarzy, poza zwierzętami, mogą występować również mikroorganizmy eukariotyczne (protisty) np.: promienice, otwornice i orzęski. W ostatnich latach wykazano również, że takie symbiotyczne układy mogą być bardziej skomplikowane i nie ograniczają się jedynie do gospodarza i symbionta, a w ich funkcjonowaniu i stabilizacji mogą brać udział dodatkowi jednokomórkowi partnerzy.
Symbiozę możemy zdefiniować jako długotrwałą relację dwóch lub więcej organizmów. Jedną z najlepiej zbadanych symbioz jest ta między koralowcami i jednokomórkowymi glonami. W tym układzie, fotosyntetyzujący symbiont wytwarza cukry, z których korzysta gospodarz, w zamian zapewniając symbiontowi schronienie. Taki rodzaj symbiozy między cudzożywnym gospodarzem i glonem nazywany jest fotosymbiozą. Jest ona powszechna w środowiskach morskich, gdzie symbiotyczne glony mają znaczny wkład w produkcję pierwotną i stanowią istotną część biomasy ekosystemów. Fotosymbiozy umożliwiają wzrost gospodarza w niekorzystnych warunkach umożliwiając mu pozyskiwanie deficytowych składników od partnera. W roli gospodarzy, poza zwierzętami, mogą występować również mikroorganizmy eukariotyczne (protisty) np.: promienice, otwornice i orzęski. W ostatnich latach wykazano również, że takie symbiotyczne układy mogą być bardziej skomplikowane i nie ograniczają się jedynie do gospodarza i symbionta, a w ich funkcjonowaniu i stabilizacji mogą brać udział dodatkowi jednokomórkowi partnerzy.
Ze względu na ewolucyjne znaczenie fotosymbiozy i jej rolę w ekosystemach wodnych rośnie liczba badań układów fotosymbiotycznych w środowiskach morskich. Jednak różnorodność tych układów oraz funkcjonowanie i ewolucja fotosymbiozy w wodach słodkich są wciąż słabo poznane, a większość badań koncentruje się na modelowym orzęsku Paramecium bursaria i jego fotosymbioncie – zielenicy z rodzaju Chlorella. Aby lepiej zrozumieć słodkowodne symbiozy, skupimy się na badaniu różnych gatunków fotosymbiotycznych orzęsków.

OPIS PROJEKTU
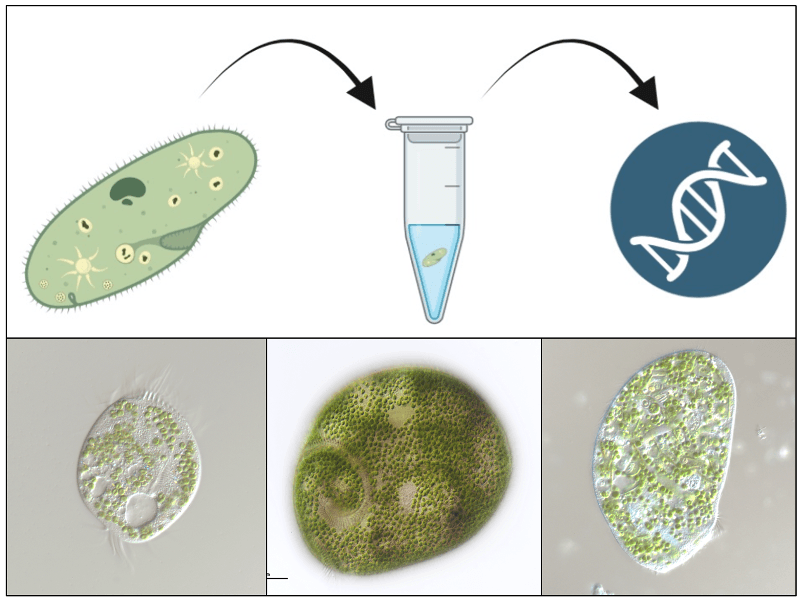
W celu poznania różnorodności fotosymbiotycznych orzęsków w wybranych środowiskach słodkowodnych wykorzystamy metody sekwencjonowania krótkich fragmentów DNA. Zbierzemy również takie dane jak dostępność składników odżywczych, temperatura wody, zawartość rozpuszczonego tlenu i dostępność światła, które umożliwią poznanie preferencji środowiskowych, poszczególnych gatunków orzęsków. Charakterystykę gospodarza, symbionta i potencjalnych dodatkowych partnerów w układzie fotosymbiotycznym umożliwi sekwencjonowanie genomów pojedynczych komórek orzęsków izolowanych ze środowiska. Analiza genomów pozwoli również określić interakcje między partnerami, w tym rodzaj i sposób wymiany składników odżywczych. Aby zrozumieć mechanizmy molekularne leżące u podstaw badanych relacji, zastosujemy sekwencjonowanie transkryptomów pojedynczych komórek gospodarzy i symbiontów. Uzyskane dane umożliwią analizę ekspresji genów i pomogą wskazać mechanizmy kontroli interakcji gospodarz-symbiont.
Przeprowadzone badania terenowe umożliwią określenie wpływu czynników środowiskowych na liczebność i różnorodność fotosymbiotycznych orzęsków słodkowodnych. Charakterystyka molekularna gospodarza, symbionta i innych partnerów pomoże zrozumieć molekularne podstawy stabilności i funkcjonowania symbiotycznych układów. Uzyskane wyniki przyczynią się do lepszego zrozumienia zjawiska fotosymbiozy i miksotrofii (czyli mieszanego sposobu odżywiania się na drodze fototrofii i heterotrofii). Jest to szczególnie istotne ze względu na rolę miksotrofów w ekosystemach wodnych w zmieniających się warunkach środowiskowych. Badania układów symbiotycznych na poziomie molekularnym przyczynią się również do lepszego zrozumienia wpływu symbioz na ewolucję eukariontów.
ZBIERANIE PRÓB
Naszym badania oparte są głównie o analizy trzech zbiorników znajdujących się w Zielonce pod Warszawą. W celu określenia, jak sezonowość wpływa na fotosymbiozy u orzęsków i zebrania pojedynczych komórki na potrzeby sekwencjonowania genomów i transkryptomów próbkowaliśmy te zbiorniki co miesiąc przez cały rok. Za każdym razem zbieraliśmy wodę do analiz chemicznych i do późniejszej filtracji oraz próby osadów i zagęszczonego planktonu na potrzeby wyciągania pojedynczych komórek. Mierzyliśmy również temperaturę i zawartość tlenu w wodzie za pomocą sondy wieloparametrowej.
Żeby zwiększyć różnorodność badanych symbioz odwiedzamy również inne zbiorniki znajdujące się w Warszawie oraz na Mazurach.

PRACA NA POJEDYNCZYCH KOMÓRKACH
Zebrane w terenie oglądamy następnie pod mikroskopem świetlnym i szukamy orzęsków posiadających w sobie zielenicowe endosymbionty. Takie orzęski są pojedynczo izolowane w celu przeprowadzenia amplifikacji całogenomowej i sekwencjonowania ich genomów i transkryptomów.
KONFERENCJE
• Chwalińska M., Karnkowska A. Photosymbiosis in freshwater ciliates: elucidating its diversity, functioning and evolution with single-cell sequencing. de.NBI Spring School 2024 – Bioinformatics for Microbial Omics. Bielefeld, Niemcy, marzec 18–22, 2024. Poster i flash talk
• Chwalińska M., Karnkowska A. Uncover the nature of ciliate-green algae symbiosis using single-cell genomics. EMBO Early Career Lecture Course “Evolutionary and Comparative Genomics”. Nafplion, Grecja, listopad 3–6, 2024. Poster
• Chwalińska M., Tymoshenko D., Archibald J., Karnkowska A. A single-cell genomic workflow for characterizing unculturable and diverse ciliate–green alga photosymbioses. EMBO | EMBL Symposium: The cellular mechanics of symbiosis: sensing friend from foe. Heidelberg, Niemcy, marzec 17-20, 2026. Poster i flash talk
• Chwalińska M., Méndez-Sánchez D., Tymoshenko D., Archibald J., Karnkowska A. Freshwater photosymbiotic ciliates – complex systems reconstructed with single-cell genomics. Protistology Open 2026. Praga, Republika Czeska, kwiecień 19-23, 2026. Prezentacja
STAŻ ZAGRANICZY
Doktorantka Małgorzata Chwalińska odbyła trzymiesięczny staż w grupie badawczej Prof. Johna Archibalda (Institute for Comparative Genomics) na Uniwersytecie Dalhousie w Halifaxie w Nowej Szkocji w Kanadzie. Staż trwał od sierpnia do listopada 2025 roku i był możliwy dzięki finansowaniu z Narodowej Agencji Wymiany Akademickiej NAWA.